Technologie d'osmose inverse (RO) est largement utilisé dans le traitement de l’eau en raison de ses avantages, tels que des taux de dessalement stables, un faible encombrement, l’automatisation et l’évolutivité. Cependant, l’entartrage constitue un problème gênant pour le personnel chargé du traitement de l’eau lors du fonctionnement des membranes. Le tartre peut entraîner une diminution du flux membranaire, une augmentation de la consommation d’énergie, des taux de dessalement plus faibles et une durée de vie réduite de la membrane, ce qui augmente les coûts opérationnels. Par conséquent, des mesures doivent être prises pour éviter le tartre de la membrane. Les méthodes courantes d'inhibition du tartre comprennent deux approches principales : l'ajustement du pH de l'eau d'alimentation RO et l'ajout d'inhibiteurs de tartre à l'eau d'alimentation. Les deux méthodes peuvent également être utilisées ensemble. Cet article traite du mécanisme d'inhibition du tartre et fournit des méthodes pour sélectionner la méthode d'inhibition et calculer la dose requise.
1. Mécanisme inhibiteur de tartre
L'entartrage de la membrane fait référence à la précipitation de substances peu solubles, telles que CaCO3, CaSO4, BaSO4 et Ca3(PO4)2, à la surface de la membrane. Lorsque ces substances se concentrent dans le système RO, elles peuvent atteindre une sursaturation. Par exemple, à un pH = 7,5 et une température de l’eau de 25 °C, lorsque la dureté calcique (mesurée en CaCO3) est de 200 mg/L et que l’alcalinité totale (mesurée en CaCO3) est de 150 mg/L, le CaCO3 approchera de la sursaturation. De même, à pH = 7,5 et à une température de l’eau de 25 °C, lorsque la concentration d’ions baryum n’est que de 0,01 mg/L et que les ions sulfate sont de 4,5 mg/L, BaSO4 deviendra sursaturé et précipitera.
Le mécanisme d’inhibition du tartre des inhibiteurs de tartre de l’osmose inverse implique principalement la complexation, la dispersion, la distorsion du réseau et les effets de seuil.
Complexation et solubilisation : les inhibiteurs de tartre peuvent former des complexes solubles avec les cations de tartre dans l'eau, tels que les ions calcium, magnésium et baryum, empêchant la formation de CaCO3, CaSO4, BaSO4 et Ca3(PO4)2.
Coagulation et dispersion : Les anions libérés par les inhibiteurs de tartre se fixent sur les cristaux de CaCO3. Étant donné que les contaminants présents dans les eaux usées industrielles portent généralement une charge négative, les charges se repoussent les unes les autres, créant une répulsion électrostatique qui empêche les cristaux de CaCO3 de s'agréger et de se développer en particules plus grosses. Les cristaux sont dispersés uniformément dans la solution, inhibant ainsi la formation de tartre de CaCO3.
Distorsion du réseau : lors de l'agrégation et de la croissance des microcristaux de CaCO3, des inhibiteurs de tartre sont incorporés dans le réseau cristallin ou à l'interface cristalline, provoquant une distorsion du réseau. Cela inhibe ou déforme directement la croissance des cristaux. Par exemple, le CaCO3 est formé d’ions calcium chargés positivement et d’ions bicarbonate chargés négativement, qui croissent dans une direction spécifique. UNu cours de leur développement, des inhibiteurs de tartre sont incorporés dans le réseau, augmentant ainsi les contraintes internes au sein du cristal. Lorsque la contrainte atteint un certain seuil, le cristal se rompt, empêchant ainsi la formation de cristaux.
Effet de seuil : Les inhibiteurs de tartre perturbent les processus d'agrégation et d'ordonnancement des microcristaux de CaCO3, CaSO4, BaSO4, Ca3(PO4)2, empêchant ainsi la précipitation.
2. Sélection des méthodes d’inhibition de mise à l’échelle
Le principal indicateur utilisé pour évaluer le risque de tartre dans les systèmes d’osmose inverse (OI) est l’indice de saturation de Langelier (LSI). Lorsque LSI < 0, l’eau n’a pas tendance à s’entartrer (même si elle peut être légèrement corrosive). Lorsque LSI ≥ 0, l’eau est sujette au tartre. La méthode d'ajustement du pH empêche le tartre en abaissant le pH de l'eau d'alimentation, déplaçant ainsi le LSI de supérieur à 0 à moins de 0. L'ajout d'inhibiteurs de tartre peut empêcher le tartre même lorsque le LSI ≥ 0, car les microcristaux insolubles dans l'eau ne peuvent pas croître, s'agréger, ou précipiter. Les principaux mécanismes de cette inhibition sont les quatre décrits ci-dessus. UNctuellement, les produits nationaux inhibiteurs de tartre peuvent garantir que les substances insolubles ne précipitent pas même lorsque LSI = 3. Les inhibiteurs internationaux de grandes marques peuvent garantir l'absence de précipitation à LSI = 5. Cependant, il est important d'être prudent lors de l'achat d'inhibiteurs, car certains fournisseurs nationaux importent concentrés d'inhibiteurs de marque internationale et les diluer avec de grandes quantités d'eau, ce qui entraîne des écarts significatifs dans les performances réelles d'inhibition du tartre, même si le produit est étiqueté comme LSI = 5.
1. Méthode d'ajustement du pH
Pour garantir la production d'eau de perméat qualifiée, le pH de l'eau d'alimentation RO est généralement contrôlé entre 6 et 9, certaines entreprises mettant en œuvre un contrôle plus raffiné dans une plage plus étroite, telle que 7,0 à 8,5. Des niveaux de pH extrêmement bas ou élevés dans l’eau d’alimentation peuvent empêcher le perméat RO de répondre aux normes de qualité de l’eau requises. Par conséquent, la méthode d’ajustement du pH pour l’inhibition du tartre suppose que le pH du perméat RO se situera dans la plage souhaitée. Il est important de noter que la méthode d’ajustement du pH cible principalement le tartre du CaCO3 et est inefficace contre d’autres types de substances calcaires.
2. Méthode d’ajout d’inhibiteur de tartre
Comme mentionné précédemment, l’ajout d’inhibiteurs de tartre peut permettre aux membranes RO de tolérer des valeurs LSI plus élevées. Cependant, les inhibiteurs de tartre RO ont tendance à être chers, les produits nationaux allant de 0,008 à 0,012 RMB/g et les produits concentrés de grandes marques internationales coûtant entre 0,055 et 0,075 RMB/g, ce qui entraîne des coûts d'exploitation élevés.
De plus, il existe de nombreux types d'inhibiteurs de tartre sur le marché, et certains fabricants promeuvent constamment de nouveaux concepts non éprouvés, ce qui entraîne une confusion lors du choix d'un inhibiteur de tartre. Généralement, les inhibiteurs de tartre commerciaux matures peuvent être classés en trois catégories : les inhibiteurs de tartre à base de phosphore, les inhibiteurs de tartre à base de polymère et les inhibiteurs de tartre respectueux de l'environnement.
-
Inhibiteurs de tartre à base de phosphore : Ceux-ci comprennent les inhibiteurs de phosphate inorganiques (tels que le tripolyphosphate de sodium ou l'hexamétaphosphate de sodium) et les inhibiteurs de phosphonates organiques (tels que l'acide hydroxyéthylidène diphosphonique, l'acide aminotriméthylènephosphonique et les dérivés de l'acide phosphonique). Les inhibiteurs de phosphate inorganiques contiennent des anions à longue chaîne et sont sujets à l'hydrolyse, en particulier à des températures plus élevées. Lorsqu'ils sont hydrolysés, ils forment des sels d'acide phosphorique, qui peuvent réagir avec les ions calcium pour former du Ca3(PO4)2, un tartre avec un produit de solubilité inférieure à celui du CaCO3. Par conséquent, les inhibiteurs de phosphate inorganiques ne conviennent pas aux eaux présentant des températures élevées ou des concentrations élevées d’ions calcium.
-
Inhibiteurs de tartre de phosphonate organique : Ces inhibiteurs contiennent des phosphonates organiques, généralement caractérisés par la liaison C-O-P. Lorsqu'ils sont exposés à des températures élevées et à des environnements alcalins, les phosphonates organiques peuvent s'hydrolyser en esters phosphoriques et en alcools, réduisant considérablement leur efficacité d'inhibition du tartre. Par conséquent, les phosphonates organiques ne conviennent pas à une utilisation dans des eaux présentant des températures ou des valeurs de pH élevées.
Les inhibiteurs de tartre à base de polymères sont principalement divisés en inhibiteurs de polymères anioniques et cationiques. Le premier est principalement utilisé pour empêcher le tartre des ions métalliques, tandis que le second est principalement utilisé pour inhiber le tartre de la silice. Les principaux ingrédients des inhibiteurs à base de polymères sont l’acide acrylique et l’acide maléique, et lors de la formulation, divers groupes fonctionnels sont introduits dans les molécules. En conséquence, les inhibiteurs de tartre polymère se présentent sous diverses formulations. Lors de l’utilisation de ces inhibiteurs, il est important de considérer non seulement les conditions de qualité de l’eau mais également les types de tartre présents. Par exemple, les inhibiteurs de polymères avec des groupes carboxyle ciblent principalement le tartre du calcium, les inhibiteurs de polymères à base d'acide sulfonique sont principalement utilisés pour le tartre des oxydes métalliques et les inhibiteurs de polymères à base d'amine sont efficaces pour le tartre de la silice. Par conséquent, les inhibiteurs de tartre polymère ne sont pas des agents à large spectre ; ils sont conçus pour combler les lacunes des inhibiteurs à large spectre. De plus, étant donné que le composant principal des inhibiteurs à base de polymères est un polymère, ils sont sensibles à l'oxydation par le chlore et d'autres biocides oxydants, ce qui peut les rendre inefficaces. Par conséquent, avant d’ajouter ces inhibiteurs, il est nécessaire de neutraliser tout chlore résiduel dans l’eau en ajoutant un agent réducteur.
Les inhibiteurs de tartre environnemental contiennent généralement des ingrédients actifs tels que l'acide polyaspartique, l'acide polyépoxysuccinique et leurs dérivés. Ces inhibiteurs sont principalement utilisés pour lutter contre les tartres à base de calcium comme CaCO3, CaSO4 et CaF2. L’avantage de ces inhibiteurs est qu’ils peuvent tolérer des concentrations d’ions calcium relativement élevées. Par exemple, même lorsque la concentration en ions calcium atteint 500 mg/L, ils peuvent toujours atteindre une inhibition de plus de 80 % du tartre calcique. Cependant, ces inhibiteurs nécessitent des dosages plus élevés, provoquent des changements importants dans le pH de l'eau et sont moins efficaces à des températures inférieures à 40°C. Étant donné que la température maximale autorisée de l'eau d'alimentation pour les membranes d'osmose inverse est de 35 à 40 °C, ces inhibiteurs ne conviennent généralement pas aux systèmes d'osmose inverse, mais sont plus couramment utilisés dans les systèmes d'eau de refroidissement.
3. Calcul de la posologie
Comme mentionné précédemment, le fait que l'eau soit sujette au tartre dépend de la valeur de l'indice de saturation de Langelier (LSI). Par conséquent, qu’il s’agisse d’utiliser un dosage d’acide pour ajuster le pH ou d’ajouter des inhibiteurs de tartre pour empêcher le tartre de la membrane d’osmose inverse, l’essentiel est de contrôler le LSI de l’eau. Le calcul du LSI est le suivant :
Dans la formule :
- pH est la valeur pH mesurée du concentré d’osmose inverse.
- pH_s est la valeur du pH de saturation correspondant au système carbonate dans l'eau à la température réelle de l'eau, appelée pH de saturation.
Le pH du concentré d’osmose inverse peut être facilement obtenu grâce à des instruments en ligne ou à une mesure manuelle. Par conséquent, la clé du calcul du LSI est de déterminer pH_s . Selon le Méthodes standard d’examen de l’eau et des eaux usées , pH_s peut être calculé à l’aide de la formule suivante.
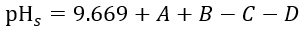
Dans la formule :
- A est le coefficient des matières dissoutes totales (DT).
- B est le coefficient de température de l’eau.
- C est le coefficient de dureté calcique.
- D est le coefficient d'alcalinité totale.
Les méthodes de calcul pour A , B , C , et D sont les suivants.

- TDS est la teneur totale en matières dissoutes dans le concentré d'osmose inverse, en mg/L.
- t est la température du concentré d'osmose inverse, en °C.
- Cca est la dureté calcique du concentré d'osmose inverse, exprimée en CaCO3, en mg/L.
- C_alcalinité totale est l'alcalinité totale du concentré d'osmose inverse, exprimée en CaCO3, en mg/L.
En utilisant l'exemple mentionné précédemment, où pH = 7,5 , TDS = 2 000 mg/L , température t = 25°C , dureté calcique Cca = 200 mg/L , et alcalinité totale C_alcalinité totale = 150 mg/L , le processus de calcul du LSI est le suivant :
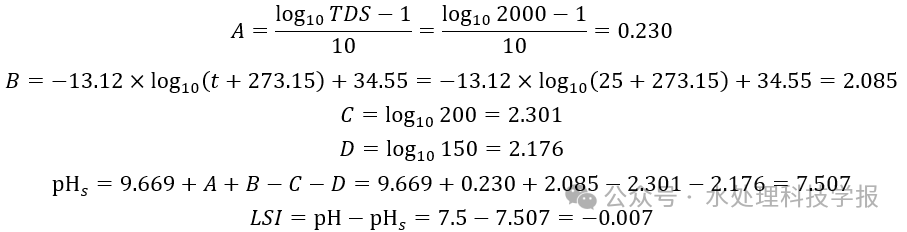
Cela concorde avec la déclaration précédente, selon laquelle dans ces conditions, le CaCO3 est presque saturé. Par ailleurs, on peut observer que le calcul du dosage peut être exprimé par les trois formules suivantes.
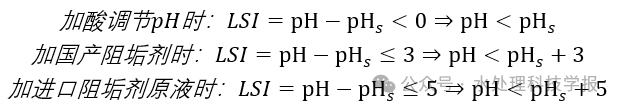
La méthode de candidature spécifique est la suivante :
Tout d'abord, nous mesurons le TDS, la température t , dureté calcique Cca , et alcalinité totale C_alcalinité totale du concentré d'osmose inverse. Ensuite, en utilisant la formule, nous calculons pH_s .
- Si pH_s ≥ pH , aucun autre ajustement ni aucun inhibiteur de tartre n'est nécessaire pour empêcher le tartre du calcium.
- Si pH_s < pH , nous veillons à ce qu'après ajustement du pH, le pH de l'eau d'alimentation par osmose inverse ne descende pas en dessous de 6,5 (puisqu'un pH inférieur peut entraîner une eau de produit d'osmose inverse acide). Dans ce cas, on peut ajuster le pH en ajoutant de l'acide jusqu'à ce que pH_s ≥ pH . Ceci n'est applicable que lorsque pH_s ≥ 6,5 . Si pH_s < 6,5 , nous devons ajuster le pH avec de l'acide jusqu'à ce qu'il atteigne 6,5 ou même moins, ce qui rendra l'eau du produit d'osmose inverse acide.
- Si pH_s < 6,5 , des inhibiteurs de tartre doivent être ajoutés.
Il est important de noter que, comme mentionné précédemment, le dosage d'acide pour l'ajustement du pH cible principalement CaCO3 mise à l’échelle et est inefficace pour les autres types de mise à l’échelle. Pour les autres substances calcaires, un antitartre est nécessaire pour le contrôle.
Pour que le dosage d'acide ajuste le pH, le dosage peut être contrôlé par le pH réellement mesuré. En ce qui concerne le dosage de l'inhibiteur de tartre, des recherches approfondies menées par des chercheurs nationaux et internationaux ont montré que :
- Lorsque la dose d’inhibiteur de tartre est inférieure 2,5 g/m³ , l'efficacité de l'inhibition est relativement faible.
- Lorsque la dose dépasse 3,0 g/m³ , l'efficacité de l'inhibition ne s'améliore plus de manière significative.
Ainsi, le dosage optimal d’inhibiteur de tartre se situe entre 2,5-3,0 g/m³ , comme le montre le tableau suivant.
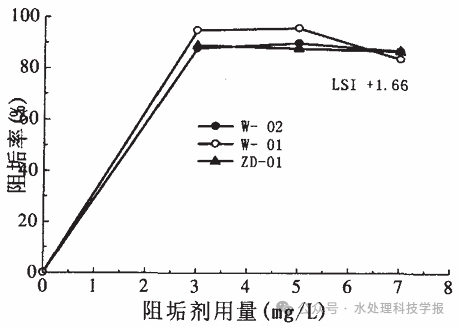
En résumé, pour éviter le tartre de la membrane d’osmose inverse, nous devons d’abord calculer le LSI du concentré d’osmose inverse à l’aide des formules fournies dans cet article pour évaluer si un tartre est susceptible de se produire. Deuxièmement, nous devons analyser les principales substances calcaires présentes dans le perméat, qui peuvent être déterminées en testant des indicateurs tels que Ca²⁺, Mg²⁺, HCO₃⁻, Ba²⁺, SiO₂, etc. Cette analyse nous permet de prendre des décisions ciblées quant à l'opportunité de ajuster le pH avec de l'acide ou ajouter des inhibiteurs de tartre. Si un inhibiteur de tartre est nécessaire, nous devons déterminer le type et la dose appropriés d’inhibiteur à utiliser.


